Immunity:我国学者揭示代谢与免疫新机制

在国家自然科学基金优秀青年科学基金(项目编号:31522020)和面上项目(项目编号:31270017)等资助下,浙江大学医学院王迪教授通过构建动物疾病模型,结合免疫学、细胞生物学和生物化学等研究手段,发现胆酸可以通过抑制NLRP3炎症小体从而改善炎症性疾病,如脓毒症、腹腔炎以及二型糖尿病等的发生,揭示了脂代谢通路蛋白参与炎症性疾病发生发展的新机制。
研究成果以“Bile Acids Control Inflammation and Metabolic Disorder through Inhibition of NLRP3 Inflammasome(胆酸通过抑制NLRP3炎症小体调控炎症和机体代谢失调)”为题于2016年10月18日在Immunity发表。论文链接: http://dx.doi.org/10.1016/j.immuni.2016.09.008。
当前人类多数顽疾均与免疫系统紊乱相关,而免疫系统受代谢系统的密切调控,免疫系统通过改变代谢显著影响代谢性疾病的进程,这使得代谢免疫学成为当今重要的新兴学科。 胆酸作为胆汁的关键组分之一, 以往被认为是重要的代谢调节物,在脂类代谢中发挥重要作用。近年来,越来越多的研究显示:胆酸还发挥着重要的激素调节作用,可以通过激活多种受体发挥复杂的生理和病理功能。
王迪教授课题组的研究发现,胆酸通过TGR5受体激活PKA激酶进而直接磷酸化NLRP3 291位点的丝氨酸,导致NLRP3的泛素化;功能实验证实,这两种PKA引起的NLRP3蛋白翻译后修饰,在抑制NLRP3炎症小体活化过程中发挥着重要的作用。同时该分子机制也有可能参与到某些NLRP3炎症小体过度活化导致的炎症性疾病的发病机制当中。
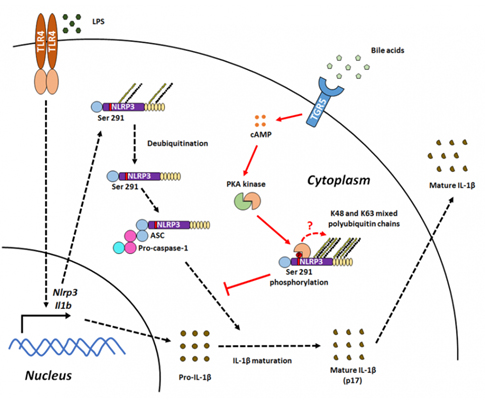
图 胆酸分子(Bile acids)通过TGR5-cAMP-PKA信号转导通路抑制NLRP3炎症小体活化
- 上一篇:基因组编辑:谁能手握第四代新“剪刀” 2016/10/28
- 下一篇:Nature免疫疗法突破:剑桥大学科学家让T细胞“活更久” 2016/10/28

